Cục Quản lý dược, Bộ Y tế vừa ban hành quyết định xử phạt hành chính đối với Amvipharm, địa chỉ tại Lô B14-3,4 Đường N13, Khu công nghiệp Đông Nam, Xã Hòa Phú, Huyện Củ Chi, TP. Hồ Chí Minh.
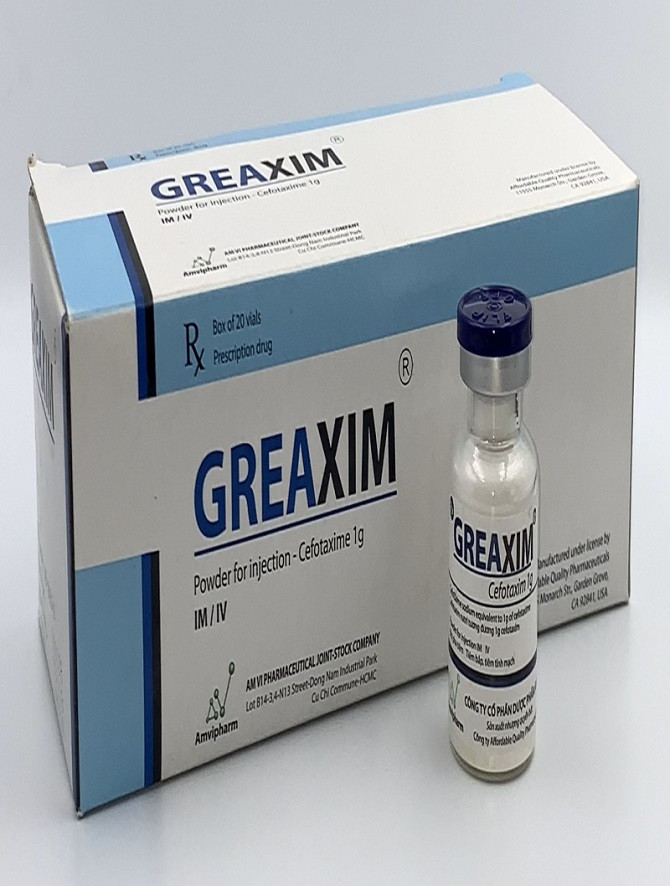
Cụ thể, theo Cục Quản lý dược, Công ty đã không kiểm nghiệm thuốc và nguyên liệu làm thuốc trước khi xuất xưởng theo quy định của pháp luật đối với 06 lô thuốc: Thuốc bột pha tiêm Greaxim 2g (Cefotaxim (dưới dạng Cefotaxim sodium) 2g, Số GĐKLH: VD-33386-19, Số lô: 060822, HD: 11.08.2024; Số lô: 070822, HD:14.08.2024; Số lô: 080822, HD: 15.08.2024; Thuốc bột pha tiêm Greaxim (Cefotaxim (dưới dạng cefotaxim natri) 1g), Số GĐKLH: VD-18235-13, Số lô: 110822, HD:08.08.2024; Số lô:120822, HD: 09.08.2024; Số lô: 130822, HD: 10.08.2024.
Greaxim là thuốc được chỉ định điều trị cho bệnh nhân mắc nhiễm khuẩn nặng và nguy kịch do vi khuẩn nhạy cảm với Cefotaxim như nhiễm khuẩn huyết, áp xe não, viêm màng trong tim, viêm phổi, bệnh lậu... Ngoài ra, thuốc cũng được sử dụng trong một số bệnh lý khác khi có chỉ định từ phía bác sĩ.
Với hành vi trên, Công ty bị áp dụng mức phạt tiền là 80 triệu đồng. Hình thức xử phạt bổ sung là đình chỉ hoạt động sản xuất thuốc Greaxim 2g (Cefotaxim (dưới dạng Cefotaxim sodium) 2g), Số GĐKLH: VD-33386-19 và thuốc Greaxim (Cefotaxim (dưới dạng cefotaxim natri) 1g), Số GĐKLH: VD18235-13. Thời gian thực hiện hình thức xử phạt bổ sung là 3 tháng, tính từ 18.1.2023.
Trước đó, tháng 11.2022, Cục Quản lý dược đã ra thông báo thu hồi 6 lô thuốc này trên toàn quốc, do xuất xưởng, đưa ra lưu hành trước khi có kết quả kiểm tra chất lượng nguyên liệu và kết quả kiểm tra chất lượng thành phẩm, vi phạm quy định tại Luật Dược.

Theo tìm hiểu, Amvipharm được thành lập năm 2010 bởi các cổ đông tại Việt Nam. Năm 2012, Công ty bắt đầu sản xuất với các sản phẩm tập trung vào thị trường bệnh viện.
Tháng 9.2015, Tập đoàn Dược phẩm CCL (Pakistan) tiếp nhận quản lý Amvipharm, hoàn tất việc sáp nhập.
Năm 2019, Công ty được trao chứng nhận “Thương hiệu vàng vì sức khỏe người Việt”, do Hội Giáo dục chăm sóc sức khỏe cộng đồng Việt Nam tổ chức.
Hiện, người đại diện theo pháp luật của Công ty là ông Amin Muhammad Jaudat, quốc tịch Pakistan làm Tổng giám đốc.